
大家好,今天分享一篇2022年发表在NATURE COMMUNICATIONS上的文章,本研究专注于创建一种通用的等温核酸扩增方法,描述了用于分析算法的抽象模型,可以应用于短核酸序列miRNAs和病原体靶标(如高突变病毒)的多路检测。

随着检测非传染性或传染性疾病的复杂生物标志物的挑战日益严峻,核酸扩增已成为功能分子分析的基石。基于等温核酸扩增分析不依赖于PCR仪一类复杂的仪器,促使上述诊断朝着即时即地方向发展。
常见的例子包括基于发夹结构的扩增系统,例如交叉引物扩增(CPA)和环介导DNA扩增(LAMP)。在这些机制中,二级发夹作为一种自折叠结构,可以打开互补的目标双链(ds) DNA,暴露其引物位点,引发下一步的引物杂交和延伸。然而,这些方法增加了设计的复杂性,忽略了作为中间产物的反应单元;为了满足对分子的多样性检测,只能开发多种不同的检测方法。
因此,作者用一套基本的指导原则,将引物设计、扩增过程与功能性扩增中间体联系起来,设计了一种通用的、简化的酶介导等温扩增方法,提出了通过创建关键中间基序(功能发夹结构)来催化扩增反应的策略。

作者开发了基于DNA节点和电路的扩增方法,整个过程被简化为五个部分。如图1A所示:功能性发卡自折叠组装过程(实心箭头);引物扩展过程(虚线箭头);通过放大产生的功能性发夹(蓝色方框);功能发卡自折叠产物(绿色三角形为正义链和绿色正方形为反义链)。整个过程围绕两个核心等温扩增反应进行,使用一个包含发夹基序(绿色三角形)的ssDNA,其在环区有一个引物结合位点,与环区互补的引物(图1A中电路S中的2a和电路A中的1s)与环区杂交时,启动延伸反应,用DNA链置换聚合酶打开发夹结构,茎上暴露的结构域(3s)作为起始位点,再次与引物结合进行延伸,产生双链产物,最后发生功能发夹自发的折叠拆卸反应(图1A的实箭头),又形成两个发卡,形成电路闭环,继续进行放大反应。图1A反应产生了长度有限的扩增子,图1D中较小的条带证实了这一点,并在图1C中通过测序证实。作者还证明了不同长度的环片段对反应动力学有着明显影响,其中环长度为40nt时,反应动力学较快(图1B)。
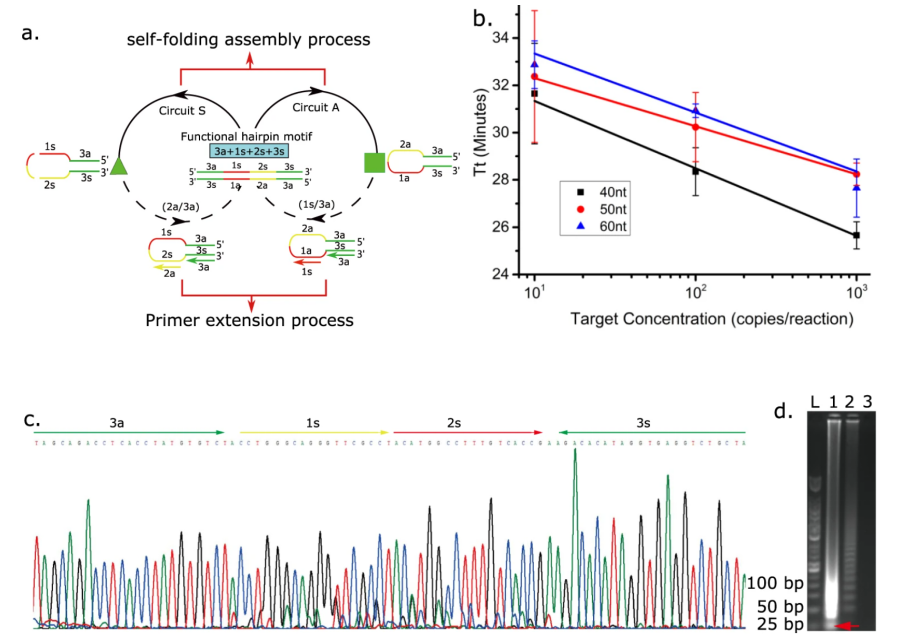
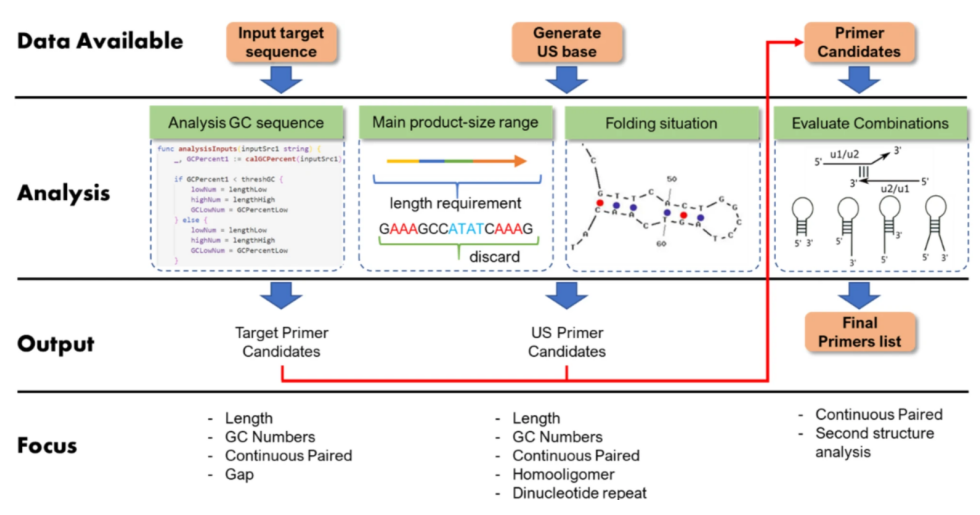
图2 引物设计软件流程图。包括(1)筛选目标序列(2)随机设计筛选US序列(3)根据四种不同方案过滤输出最终引物。
策略1:尾巴策略
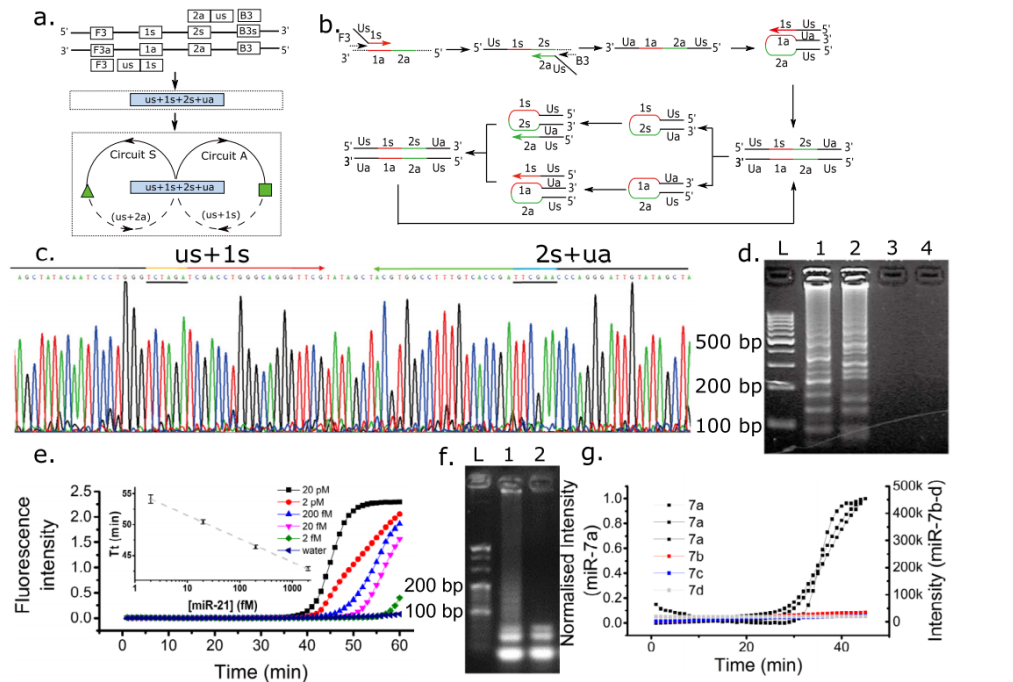
如图3A所示,通过正向引物和反向引物合成一个通用尾巴(称为us),其5’端具有相同的序列,3’端与特定的目标序列互补,产生一个功能性发夹基序(us+1s+2s+ua),然后通过DNA聚合酶进行引物延伸;另外还添加了两个外部引物(F3,B3),与在传统LAMP系统中使用的策略类似,增加了反应的动力学,达到指数放大的效果,图3B是分子反应过程的二级结构示意图。此方法可用于扩增病原体的序列,图3C证明其特殊结构的形成;图3D证实在无靶标的情况下不产生扩增子,有靶标的情况下才开始扩增。此方法也可以直接应用于短小序列的检测,并通过浓度依赖的方式(低至fM浓度)检测miR21 microRNA(图3E)。作者还检测了更广泛的miR-7家族,证明该方法能够从同一家族的其他成员中检测低浓度的miR-7-a(图3G)。
策略2:递进模型
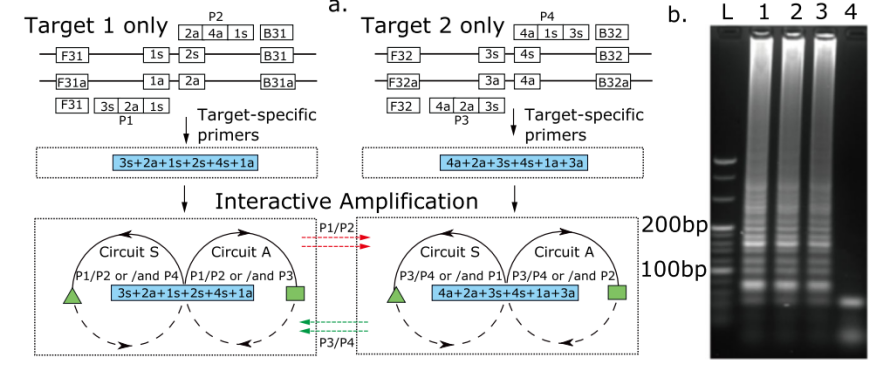
当将额外的反应途径连接到主要途径时一般会出现复杂性的增加,例如EXPAR中扩增途径的一个产物作为第二个反应的输入。作者提出的第二种策略就是用来克服这种复杂性增加。利用中间体作为不同反应途径之间的链接,设计了一个等温扩增体系,该体系含有一个与目标序列3端互补的正向引物(3a+1s),与目标单个序列互补的反向引物(2a、3a、4a和5a),生成三个不同的功能发夹,这些发卡都包含相同的基序(3a+1s+2s+3s)。引物延伸过程中,引物2a/3a+1s分别结合在正义链和反义链环区,延伸后导致发夹结构打开,暴露出其他引物结合位点。关键中间结构可形成渐进式模型,驱动指数放大过程,如发夹(3a+1s+2s+3s+4s+5s)有两种功能,既可以与引物2a/4a和2a/3a在电路S1中催化生成3a+1s+2s+3s+4s和3a+1s+2s+3s,也可与引物2a/5a在电路S1和电路A1上都产生一个新的拷贝,从而起到递进放大的效果。作者也评估了这个渐进模型的敏感性,如图5B所示,随着目标浓度的增加,反应速度加快。图5C也证实,含有反义引物5a+4a和4a的系统比只使用引物3a的系统快,这是因为随着反义引物序列的引入,不同的扩增通路可被激活,有更多的机会形成更有功能的发夹,使反应动力学呈指数级变化。
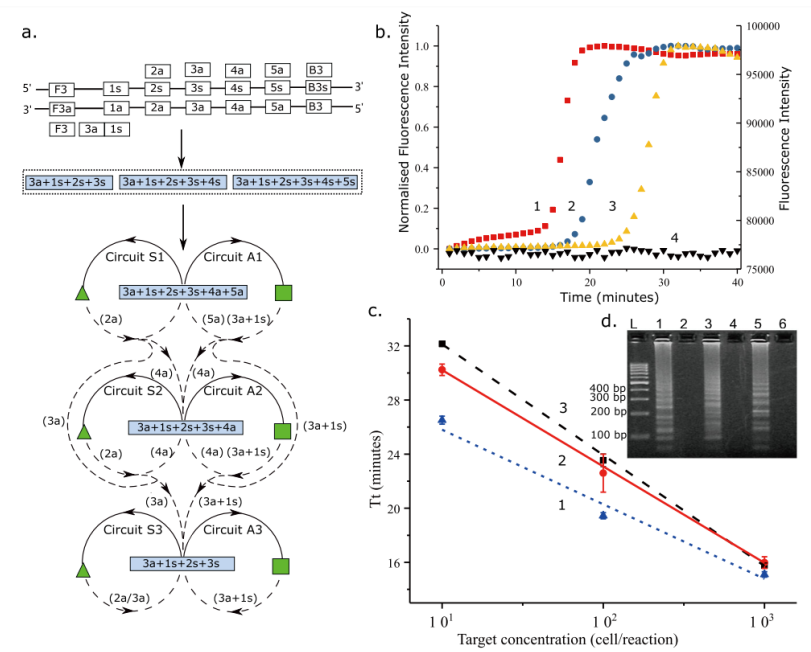
图5 具有指数动力学的递进模型。
A 反应原理图。多个中间体形成(3a+1s+2s +3s, 3a+1s+2s+3s+4s, 3a+1s+2s+3s+ 5s)。
B 10倍连续稀释靶标的递进模型实时放大曲线:400 M结核细胞(红方);40M结核细胞(蓝圈);4M结核细胞(黄色三角形);阴性对照(黑色三角形)。
C 实时检测引入不同反义引物体系的动力学:3a + 4a + 5a(蓝点);3a + 4a(红线);3a(黑色破折号)。阈值时间(Tt)为产生最大荧光强度20%的时间。
D 琼脂糖凝胶电泳显示不同数量的反义引物对反应的影响。lane1/2:3a + 4a + 5a;lane3/4:3a + 4a;lane5/6:3a。lane1/3/5用40M肺结核细胞;lane2/4/6是阴性对照。



Jonathan M. Cooper,格拉斯哥大学生物工程学教授和前副校长,获得ERC高级研究员奖。专注于在生命科学界面中使用微技术和纳米技术(特别是在高级诊断和芯片实验室领域)的研究。在Nature Communication、JACS、ACS nano等高水平杂志发表多篇成果。

Julien Reboud,格拉斯哥大学生物医学工程研究员,主要研究方向为微流体、声学、诊断。在Angewandte Chemie International Edition、lab on a chip、nano letters等高水平杂志发表多篇成果。

樊春海,上海交通大学化学化工学院客座教授,国家转化医学中心执行主任,中国科学院院士(CAS院士),美国科学促进会(AAAS)、英国皇家化学学会(FRSC)、美国医学与生物工程学会(AIMBE)和国际电化学学会(ISE)的会员。ACS应用材料杂志副主编、ChemPlusChem编辑委员会联合主席。主要研究方向为双传感器、DNA纳米技术、生物光子,在同行评审期刊上发表论文500余篇。

DOI: 10.1038/s41467-022-29628-3
投稿:韩小乐
编辑:吴优
审核:杨宇君
文章评论